Nội dung bài viết
Axit Perchloric là gì? Tên HCLO4 cùng với cấu trúc phân tử của Axit Perchloric và tính chất hóa lý của Axit Perchloric là gì? Cũng như cách điều chế Axit Perchloric, công dụng của Axit Perchloric là gì? Cuối cùng, chúng tôi sẽ đề cập đến độ an toàn của hóa chất HCLO4 và mua hóa chất này ở đâu trong bài viết này!
Axit PERCLORIC LÀ GÌ?
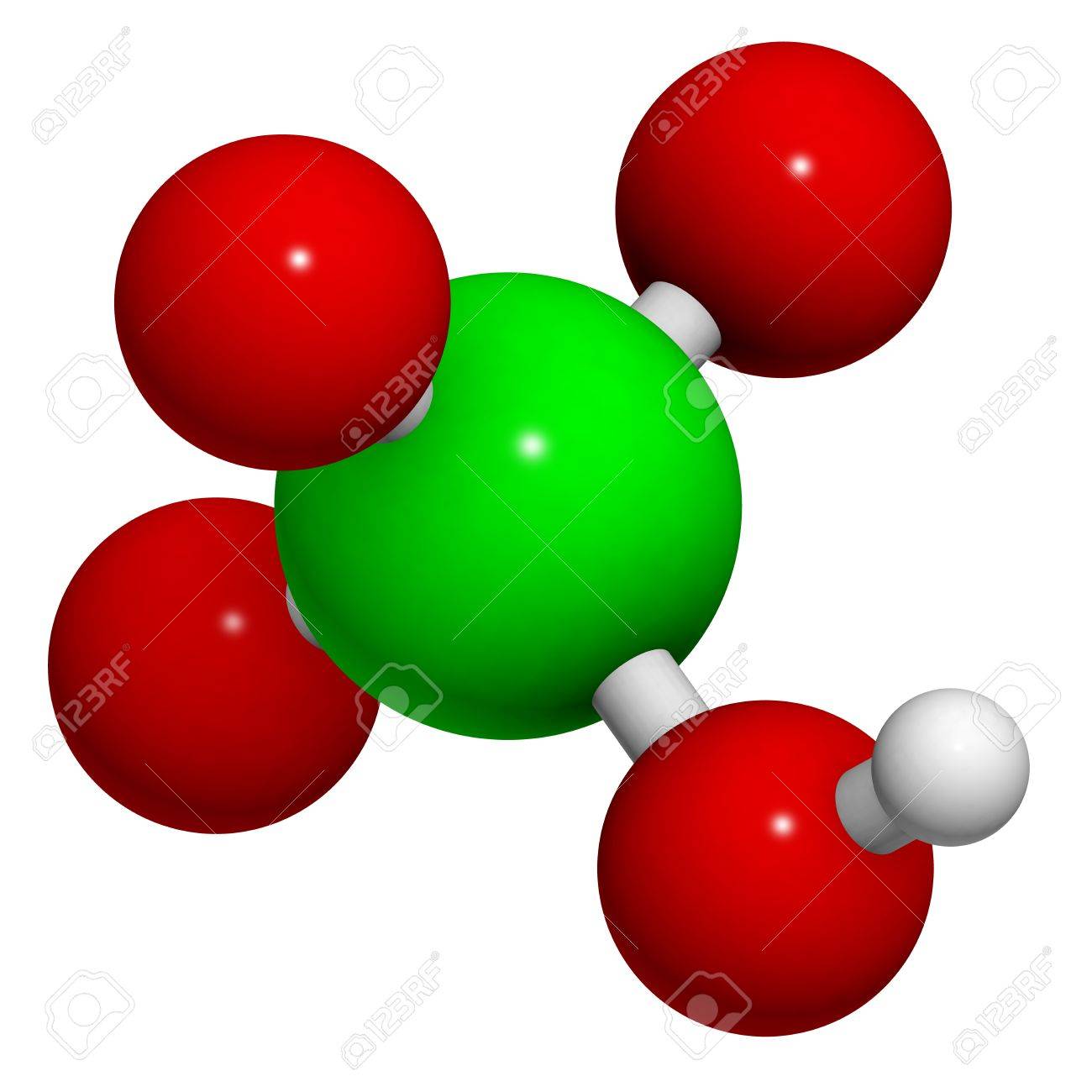 Axit PERCLORIC LÀ GÌ?
Axit PERCLORIC LÀ GÌ?
Axit perchloric là một hợp chất vô cơ có công thức hóa học HClO4. Thường ở dạng lỏng, không màu. Chất này là axit rất mạnh so với axit sunfuric và axit nitric, đồng thời cũng là chất oxy hóa mạnh; Rất tan trong nước và tạo thành với nước hydrat HClO4.nH2O (n = 1, 2 và 3). HCLO4 khan rất không ổn định nên sẽ bị phân hủy dưới áp suất thường; Khi đun nóng đến 100 độ C, nó sẽ hóa lỏng thành màu nâu đỏ và gây nổ. Axit perchloric được sử dụng để phân hủy quặng phức tạp; phân tích khoáng sản; như một chất xúc tác. Muối của axit pecloric là peclorat.
Axit perchloric, với hơn 50% nhưng không quá 72% axit xuất hiện dưới dạng dung dịch nước trong suốt, không màu, không mùi. Ăn mòn kim loại và mô. Các thùng chứa kín có thể bị vỡ dữ dội khi tiếp xúc với nhiệt độ kéo dài.
CẤU TRÚC PHÂN TỬ CỦA ACID PERCLORIC
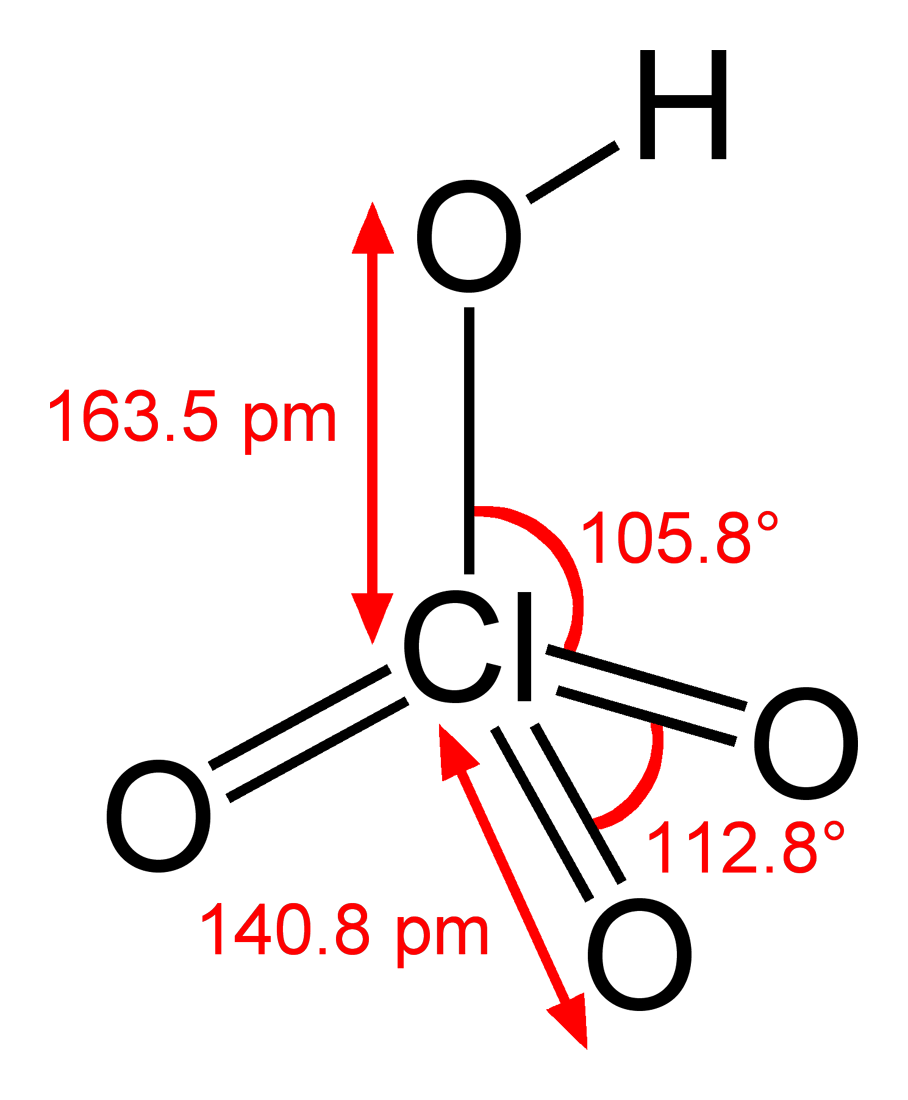 Cấu trúc phân tử của Axit Perchloric
Cấu trúc phân tử của Axit Perchloric
TÍNH CHẤT VẬT LÝ HÓA HỌC CỦA ACID PECLORIC
Tính chất vật lý của axit Perchloric
-
- Khối lượng mol 100,46 g/mol
- Xuất hiện chất lỏng không màu
- Mật độ 1,67 g/cm3
- Điểm nóng chảy -17 °C (azeotrope) và -112 °C (khan)
- Điểm sôi 203 °C (hỗn hợp đẳng phí)[2]
- Độ hòa tan trong nước hòa tan
- Độ axit (pKa) ≈ −8[3]
Tính chất hóa học của axit Perchloric
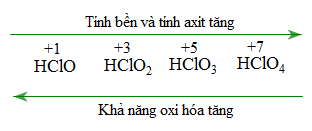 Tính chất hóa lý của axit Perchloric
Tính chất hóa lý của axit Perchloric
Phản ứng oxi hóa khử khi tiến hành nhiệt phân Axit Perchloric với chất xúc tác là nhiệt độ và P2O5 -> Khí sủi bọt tạo thành bởi dichlor heptoxide (Cl2O7).
2HClO4 → H2O + Cl2O7
Ngoài ra, HCLO4 còn tác dụng với nhiều chất theo PTPU dưới đây:
HClO4 + NH2OH ⟶ NH3OHClO4
PH3 + HClO4 ⟶ PH4ClO4
HClO4 + HF ⟶ H2O + ClO3F
P2O5 + 6HClO4 ⟶ 3Cl2O7 + 2H3PO4
KOH + HClO4 ⟶ H2O + KClO
NaOH + HClO4 ⟶ H2O + NaClO4
2F2 + 4HClO4 ⟶ 2H2O + O2 + 4ClO3F
Cs2CO3 + 2HClO4 ⟶ H2O + CO2 + 2CsClO4
Ghi chú:
Tính axit: thường được xem xét trong môi trường dung môi của nước. Phụ thuộc vào độ bền liên kết HO (khả năng phân ly H+), thường được biểu thị qua chỉ số pKa (Hằng số phân ly axit).
-
- HClO < HClO2 < HClO3 < HClO4 (Tăng O (không tham gia HO) làm tăng độ phân cực của liên kết HO).
Tính oxi hóa: HCl không có khả năng oxi hóa (Vì clo có số oxi hóa thấp nhất). Ở dãy chất còn lại, tính oxi hóa phụ thuộc vào độ ổn định phân tử. Chất càng kém bền thì khả năng oxi hóa càng cao:
-
- HClO > HClO2 > HClO3 > HClO4 (số O tăng tăng độ bền (do tăng bội số liên kết), giảm tính oxi hóa)
Bạn có thể xem thêm: Kali iodide là gì? Những điều cần biết về Kali iodide
CHUẨN BỊ AXIT PECLORIC
 CHUẨN BỊ AXIT PECLORIC
CHUẨN BỊ AXIT PECLORIC
Điều chế trong công nghiệp
Axit perchloric được điều chế công nghiệp theo hai cách.
Phương pháp thứ nhất: Cho natri peclorat phản ứng với axit clohiđric tạo thành axit percloric và kết tủa trắng của natri clorua:
NaClO4 + HCl → NaCl + HClO4
Cách thứ hai: Axit đậm đặc có thể được tinh chế bằng cách chưng cất. Trực tiếp hơn và không sử dụng thuốc thử muối, nó tạo ra quá trình oxy hóa anốt của dung dịch nước clo ở điện cực bạch kim.
Chuẩn bị trong phòng thí nghiệm
Phản ứng hóa học giữa bari perchlorate và axit sulfuric tạo ra kết tủa bari sunfat và axit perchloric.
-
- Ba(ClO4)2 + H2SO4 → BaSO4 + 2HClO4
Ngoài ra, người ta cũng có thể điều chế axit perchloric bằng cách cho axit nitric phản ứng với amoni perclorat. Phản ứng này tạo ra oxit nitơ và axit perchloric.
ỨNG DỤNG CỦA ACID PERCLORIC LÀ GÌ?
 Những công dụng của Axit Perchloric là gì?
Những công dụng của Axit Perchloric là gì?
Ứng dụng công nghiệp
Axit perchloric được điều chế hàng năm lên tới hàng triệu tấn với công dụng chính là tạo ra amoni perchlorate, chất này dùng làm nhiên liệu tên lửa.
Ứng dụng trong hóa học
Axit perchloric, là một trong những axit mạnh nhất theo. Vì vậy, không cần có các muối có khả năng phản ứng như sunfat hoặc clorit trong axit sunfuric và axit clohydric. Mặc dù có khả năng gây nổ cao khi sử dụng muối perchlorate nhưng axit perchloric vẫn được sử dụng trong nhiều quá trình tổng hợp. Vì lý do tương tự, axit cũng là dung môi hữu ích trong sắc ký trao đổi ion.
Axit perchloric cũng được sử dụng trong khắc và khắc trên nhôm, molypden và một số kim loại khác.
AN TOÀN CỦA HÓA CHẤT ACID PERCLORIC
Cảnh báo nguy hiểm
-
- H271 Có thể gây cháy, nổ; chất oxy hóa mạnh.
- H290 Có thể ăn mòn kim loại.
- H302 Có hại nếu nuốt phải.
- H314 Gây bỏng da nghiêm trọng và tổn thương mắt.
- H373 Có thểgây tổn thương các cơ quan (Tuyến giáp) khi phơi nhiễm kéo dài hoặc lặp đi lặp lại.
Lưu ý phòng ngừa
Tránh xa các nguồn nhiệt.
-
- Cẩn thận tránh trộn lẫn với các chất dễ cháy, hợp chất kim loại nặng, axit và kiềm.
- Đeo găng tay bảo hộ/quần áo bảo hộ/bảo vệ mắt/bảo vệ mặt.
- NẾU NUỐT PHẢI: Súc miệng. KHÔNG gây nôn.
- NẾU DÍNH VÀO MẮT: Rửa kỹ bằng nước trong vài phút. Tháo kính áp tròng nếu bạn đang đeo chúng và việc này rất dễ thực hiện. Tiếp tục giặt.
- Nếu bị phơi nhiễm hoặc có lo ngại: Hãy gọi ngay cho TRUNG TÂM CHỐNG ĐỘC hoặc bác sĩ
Xem thêm bài viết: Vôi sống là gì? CaO là gì? Phân biệt Vôi sống – Vôi tôi – Đá vôi
MUA ACID PERCLORIC Ở ĐÂU UY TÍN, CHẤT LƯỢNG
 Mua Axit Perchloric ở đâu uy tín, chất lượng
Mua Axit Perchloric ở đâu uy tín, chất lượng
Axit perchloric là một loại hóa chất khá phổ biến và có nhiều ứng dụng quan trọng nên nhu cầu về loại hóa chất này rất lớn. Và chính vì điều đó đặt ra một câu hỏi lớn cho khách hàng: làm thế nào để chọn mua được axit perchloric – HCLO4 chất lượng từ nhà cung cấp uy tín?
Hôm nay chúng tôi sẽ giới thiệu đến các bạn nhà cung cấp hóa chất axit perchloric – HCLO4 với chất lượng cực tốt, giá cả cạnh tranh cũng như nguồn gốc xuất xứ rõ ràng. Công ty Trường Cao Bá Quát – Nhà cung cấp hóa chất tinh khiết và dụng cụ thí nghiệm hàng đầu khu vực phía Nam.
Vui lòng liên hệ hotline (028) 3811 9991 để nhận được báo giá hóa chất axit perchloric nhanh nhất. Hoặc truy cập https://tschem.com.vn/ để tham khảo thêm các sản phẩm khác nếu bạn có nhu cầu.
Trên đây là những thông tin liên quan đến hóa chất Axit perchloric là gì? Công thức cấu tạo của hclo4 là gì? Những tính chất nào đặc trưng cho axit Perchloric hóa học? Làm thế nào để điều chế axit perchloric? Công dụng của hóa chất axit perchloric này là gì? Và hóa chất Axit Perchloric được cung cấp ở đâu?
Hy vọng nó có thể giúp ích cho bạn trong quá trình tìm hiểu về loại hóa chất này. Nếu có thắc mắc gì liên quan đến axit hclo4 vui lòng để lại bình luận để nhận được sự hỗ trợ từ công ty chúng tôi.
Đầu vào .wpcf7-form-control-wrap{border-radius:5px;box-shadow:none} .wpcf7-form-control{border-radius:5px;box-shadow:none} đầu vào[type=”submit”]đầu vào[type=”submit”].button, đầu vào[type=”submit”].chính {bán kính đường viền: 5px} .wpcf7-spinner{display:none}


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn