Nội dung bài viết
Axit sulfuric là gì? Axit sunfuric Cấu trúc phân tử của nó là gì, nó tồn tại ở dạng nào, tính chất vật lý và hóa học của nó là gì và nó được điều chế như thế nào? Và axit sulfuric có những ứng dụng gì? Bạn có cần chú ý điều gì khi sử dụng sản phẩm này hay có biện pháp bảo quản, phòng ngừa nào để sử dụng hóa chất này an toàn hơn? Hôm nay công ty Trường Cao Bá Quát sẽ thông báo tới các bạn những kiến thức trên.
Axit sunfuric là hóa chất hàng đầu, được mệnh danh là “vua hóa chất” được sử dụng trong nhiều ngành sản xuất với vai trò là nguyên liệu thô hoặc chất xúc tác chính. Hàng năm các nước trên thế giới sản xuất ra khoảng 160 triệu tấn H2SO4. H2SO4 được sử dụng để sản xuất phân bón, thuốc trừ sâu, chất tẩy rửa tổng hợp, sợi hóa học, nhựa, sơn, v.v.
Tại sao lại có tên gọi như vậy, hãy cùng Trường Cao Bá Quát tìm hiểu ngay sau đây nhé!
Axit sunfuric là gì? CẤU TRÚC PHÂN TỬ H2SO4
Axit sunfuric là gì?
Axit sunfuric tên của nó bắt nguồn từ một từ tiếng Pháp axit sulfuric
Axit sunfuric – H2SO4là chất lỏng giống dầu, không màu, không mùi, không bay hơi, nặng hơn nước gần 2 lần (98% H2SO4 có D = 1,84 g/cm3). Nó là một axit vô cơ mạnh và hòa tan hoàn toàn trong nước ở bất kỳ tỷ lệ nào.
Đặc biệt, H2SO4 tinh khiết hoàn toàn không thể tìm thấy trên Trái đất do áp suất rất lớn giữa axit sunfuric và nước. Ngoài ra, axit sunfuric còn là thành phần của mưa axit, được hình thành từ quá trình oxy hóa sulfur dioxide trong nước hoặc axit sunfuric bị oxy hóa.
Công thức phân tử: H2SO4
Cấu trúc phân tử H2SO4
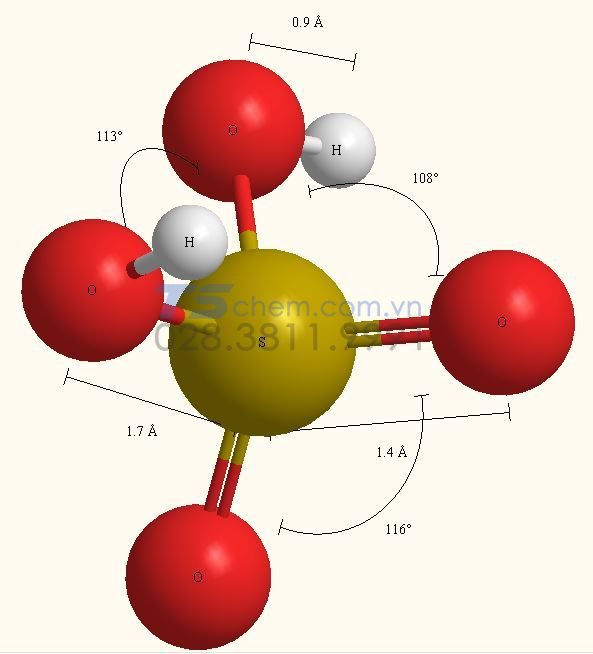 Cấu trúc phân tử H2SO4
Cấu trúc phân tử H2SO4
CÁC DẠNG Axit Sunfuric
Axit sulfuric được sử dụng với nhiều mục đích khác nhau nên sẽ tồn tại ở các dạng khác nhau như:
-
- Axit sulfuric loãng dùng trong phòng thí nghiệm thường chỉ có nồng độ 10%
- Dùng cho pin khoảng 33,5%
- Hàm lượng 62,18% là axit dùng để sản xuất phân bón
- 77,67% được sử dụng trong tháp sản xuất hoặc axit găng tay
- 98% là axit đậm đặc
TÍNH CHẤT CỦA H2SO4
Tính chất vật lý
- Axit sunfuric là chất lỏnghơi nhớt và nặng hơn nước, khó bay hơi và tan vô hạn trong nước
- Axit sulfuric đậm đặc Nó thường hút nước mạnh và tỏa nhiều nhiệt nên khi pha loãng phải cho từ từ axit đậm đặc vào nước, không làm ngược lại, vì H2SO4 có thể gây bỏng.
- Axit sunfuric Nó cũng có khả năng cacbon hóa các hợp chất hữu cơ.
Tính chất hóa học
Đối với H2SO4 lỏng
– Axit sunfuric là một axit mạnh, hóa chất này có đầy đủ các tính chất hóa học chung của axit như:
– Axit sunfuric H2SO4 làm quỳ tím chuyển sang màu đỏ.
– Phản ứng với kim loại đứng trước H (trừ Pb) tạo thành muối sunfat:
Fe + H2SO4 → FeSO4 + H2
– Phản ứng với oxit bazơ tạo thành muối mới (trong đó kim loại giữ nguyên hóa trị) và nước
FeO + H2SO4 → FeSO4 + H2O
– Axit sunfuric tác dụng với bazơ tạo thành muối và nước mới
H2SO4 + NaOH → NaHSO4 + H2O
H2SO4 + 2NaOH → Na2SO4 + 2H2O
– H2SO4 phản ứng với muối tạo thành muối mới (trong đó kim loại vẫn giữ nguyên hóa trị) và axit mới
Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2
H2SO4 + 2KHCO3 → K2SO4 + 2H2O + 2CO2
Đối với H2SO4 đậm đặc
Axit sulfuric đậm đặc có tính axit mạnh, tính oxi hóa mạnh với các tính chất hóa học nổi bật như:
– Tác dụng với kim loại: Khi cho miếng Cu vào H2SO4 sẽ tạo ra dung dịch màu xanh lam và có khí thoát ra có mùi rất nồng.
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
– Phản ứng với phi kim tạo thành oxit phi kim và nước, giải phóng khí SO2
C + 2H2SO4 → CO2 + 2H2O + 2SO2 (nhiệt độ)
2P + 5H2SO4 → 2H3PO4 + 5SO2 + 2H2O
– Tác dụng với các chất khử khác:
2FeO + 4H2SO4 → Fe2(SO4)3 + SO2 + 4H2O
– H2SO4 còn có tính chất ưa nước đặc trưng như cho H2SO4 vào cốc đường, sau phản ứng đường sẽ chuyển sang màu đen và phun trào theo phương trình hóa học sau:
C12H22O11 + H2SO4 → 12C + H2SO4.11H2O
Tham khảo thêm các bài viết khác: (FeSo4) Sắt sunfat là gì? Thuộc tính, Ứng dụng, lưu ý khi sử dụng & bảo quản
PHƯƠNG PHÁP CHUẨN BỊ H2SO4
FeS2 hoặc S → SO2 → SO3 → H2SO4
– Đốt quặng sắt firit:
-
- 4FeS2 + 11O2 → 8SO2 + 2Fe2O3
– Oxy hóa SO2 bằng oxy ở điều kiện 400 – 500 độ C, xúc tác V2O5):
-
- 2SO2 + O2 → 8SO3
– Axit sulfuric đậm đặc hấp thụ SO3 tạo thành ôle có công thức chung H2SO4.nSO3:
-
- nSO3 + H2SO4 → H2SO4 .nSO3
– Pha loãng ôle thành axit sunfuric với lượng nước thích hợp:
-
- H2SO4 .nSO3 + (n+1) H2O→ (n+1)H2SO4
ỨNG DỤNG CỦA H2SO4
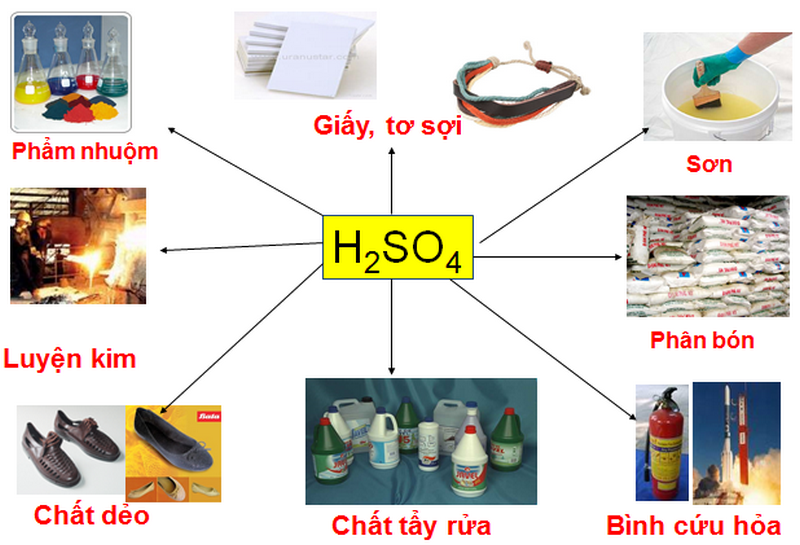 ỨNG DỤNG CỦA H2SO4
ỨNG DỤNG CỦA H2SO4
Trong sản xuất công nghiệp
Mỗi năm có khoảng 160 triệu tấn H2SO4, trong đó nó được sử dụng chủ yếu trong ngành sản xuất luyện kim 2%, thuốc nhuộm 2%, nhựa 5%, chất tẩy rửa 14%, giấy, sợi 8%…
- Axit sulfuric được sử dụng rộng rãi trong các quy trình sản xuất kim loại như sản xuất đồng, kẽm và được sử dụng trong việc làm sạch bề mặt thép và các giải pháp loại bỏ rỉ sét.
- Ngoài ra, axit sulfuric còn được dùng để sản xuất nhôm sunfat (ví dụ như phèn làm giấy). Sản xuất muối sunfat, làm sạch kim loại trước khi mạ, sản xuất thuốc nổ, nhựa, thuốc nhuộm và sản xuất dược phẩm.
- Hỗn hợp axit và nước được sử dụng làm chất điện phân trong nhiều loại pin, axit chì…
Trong phòng thí nghiệm
Điều chế các axit yếu khác: HNO3, HCL
Trong xử lý nước thải
Sản xuất nhôm hydroxit là chất được sử dụng trong các nhà máy xử lý nước để lọc tạp chất, cải thiện mùi vị của nước, trung hòa độ pH trong nước và dùng để loại bỏ các ion Mg2+, Ca2+ trong nước thải.
Trong sản xuất phân bón
Axit sulfuric (60% sản lượng của thế giới) chủ yếu được sử dụng trong sản xuất axit photphoric, được sử dụng để sản xuất phân lân, canxi dihydrogen photphat, amoni photphat và cũng để sản xuất Amoni sunfat.
Các công dụng khác của Axit Sunfuric
Sản xuất nhôm sunfat, được gọi là phèn làm giấy. Nó có thể phản ứng với một lượng nhỏ xà phòng trên sợi bột giấy để tạo ra carboxylate nhôm dạng gelatin, làm đông tụ sợi bột giấy thành bề mặt giấy cứng.
Tham khảo bài viết: Axit Citric – C6H8O7 là gì? Tính chất lý hóa, điều chế và ứng dụng
LƯU Ý KHI SỬ DỤNG Axit Sunfuric
 LƯU Ý KHI SỬ DỤNG Axit Sunfuric
LƯU Ý KHI SỬ DỤNG Axit Sunfuric
Bạn cần biết những nguy cơ tiềm ẩn của dung dịch Acid này để có thể sử dụng một cách an toàn nhất.
-
- Axit sunfuric H2SO4 rất nguy hiểm, bắn vào da có thể gây bỏng nặng, bắn vào mắt có thể gây mù, vật liệu giấy, vải sẽ cháy nếu tiếp xúc với H2SO4.
- Khi đun nóng axit sunfuric sẽ xuất hiện khí SO2, SO3. Đây là những loại khí rất độc hại.
- Khi cần pha loãng Axit Sunfuric H2SO4, tuyệt đối không cho nước vào axit trước mà luôn thêm từ từ H2SO4 vào nước.
- H2SO4 đậm đặc hút ẩm cực mạnh nên là chất làm khô tốt, áp suất hơi nước lên H2SO4 là 0,003mmHg.
- Ở nhiệt độ 30 – 40 độ C bắt đầu bốc khói và khi đun nóng thêm sẽ tạo ra hơi SO3. Quá trình sôi bắt đầu ở 290 độ C và nhiệt độ sẽ tăng nhanh cho đến khi ngừng giải phóng SO3. Hydrat còn lại chứa 98,3% H2SO4 và sôi ở nhiệt độ 338 độ C.
- Khi nguội sẽ chuyển thành tinh thể axit sunfuric H2SO4 rắn, tan chảy ở nhiệt độ 10,49 độ C. Tuy nhiên, axit lỏng có thể dễ dàng đông cứng chậm và không đông đặc ở nhiệt độ dưới 0 độ C.
BIỆN PHÁP BẢO QUẢN VÀ PHÒNG NGỪA
 Hóa chất H2SO4
Hóa chất H2SO4
Để bảo quản
-
- Bảo quản Axit Sulfuric trong thùng nhựa và thùng nhựa. Không bảo quản trong các thùng làm bằng nhôm, sắt, inox, kẽm vì đây là chất ăn mòn kim loại rất mạnh. Thùng sắt lớn chứa H2SO4 phải được phủ lớp PU. Đóng chặt nắp và đặt ở nơi khô ráo, tránh xa những nơi chứa bazơ hoặc chất khử.
- Tránh đặt gần các kim loại, kim loại nhẹ, chất có tính axit để tránh gây cháy nổ như HCl, axit nitric, axit photphoric… rất nguy hiểm.
biện pháp phòng ngừa
-
- Đây là hóa chất nguy hiểm, tiếp xúc với da sẽ gây bỏng nặng, tiếp xúc với mắt sẽ gây tổn thương mắt vĩnh viễn nên phải tránh tiếp xúc trực tiếp. Không uống hoặc hít vào.
- Khi sử dụng hoặc bơm vào bể phải mặc quần áo bảo hộ để bảo vệ cơ thể và đeo khẩu trang chuyên dụng để bảo vệ mắt. Khi vận chuyển trên đường phải sử dụng xe tăng được cấp phép an toàn.
- Không để axit chảy vào hệ thống thoát nước.
- Nếu có rò rỉ, nơi nguy hiểm phải được cách ly. Người không liên quan hoặc không mặc đồ bảo hộ không được vào nơi nguy hiểm.
- Khi cần thiết có thể dùng rào nhựa hoặc rào chắn an toàn để ngăn axit tràn ra ngoài.
MUA Ở ĐÂU UY TÍN, CHẤT LƯỢNG ACID
 MUA Ở ĐÂU UY TÍN, CHẤT LƯỢNG ACID
MUA Ở ĐÂU UY TÍN, CHẤT LƯỢNG ACID
Nếu bạn đang có nhu cầu mua sản phẩm Axit sunfuric trên thị trường, đừng bỏ lỡ nó Công ty TRUNG SƠN. Chúng tôi là một trong những địa chỉ tin cậy chuyên cung cấp hóa chất công nghiệp, hóa chất tinh khiết uy tín. Bạn sẽ không tìm được nơi nào cung cấp sản phẩm chất lượng, nguồn gốc uy tín như công ty chúng tôi. Ngoài ra, bạn còn sẽ nhận được sự tư vấn nhiệt tình từ đội ngũ nhân viên lành nghề và vô cùng nhiệt tình. Hãy đến với công ty chúng tôi nếu bạn có nhu cầu.
Hy vọng qua bài viết này các bạn có thể nhớ hoặc biết được Axit sunfuric Đó là cái gì vậy? Cũng như những vấn đề đi kèm xung quanh nó như tính chất lý hóa, cấu trúc, cách điều chế, sử dụng và bảo quản loại hóa chất này. Nếu bạn vẫn còn băn khoăn về hóa chất này, vui lòng để lại bình luận bên dưới bài viết để nhận được sự hỗ trợ từ nhân viên Trường Cao Bá Quát.
Cảm ơn bạn đã theo dõi bài viết này.
Tìm hiểu thêm trong bài viết: Toluene là gì? Tính chất, công dụng, cách bào chế & lưu ý khi sử dụng
Đầu vào .wpcf7-form-control-wrap{border-radius:5px;box-shadow:none} .wpcf7-form-control{border-radius:5px;box-shadow:none} đầu vào[type=”submit”]đầu vào[type=”submit”].button, đầu vào[type=”submit”].chính {bán kính đường viền: 5px} .wpcf7-spinner{display:none}


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn